Sicherstellung von Qualität und FDA-Zulassungen durch unsere Beratung
Der Medical Device 510 (K) Approval Prozess kann für Hersteller von medizinischen Geräten eine wichtige Voraussetzung darstellen, um Ihre Produkte auf den US-Markt zu bringen. Durch die Erfüllung der Anforderungen der FDA können Sie sicherstellen, dass ihre Geräte sicher und wirksam sind und den hohen Standards der US-Regulierungsbehörde entsprechen.
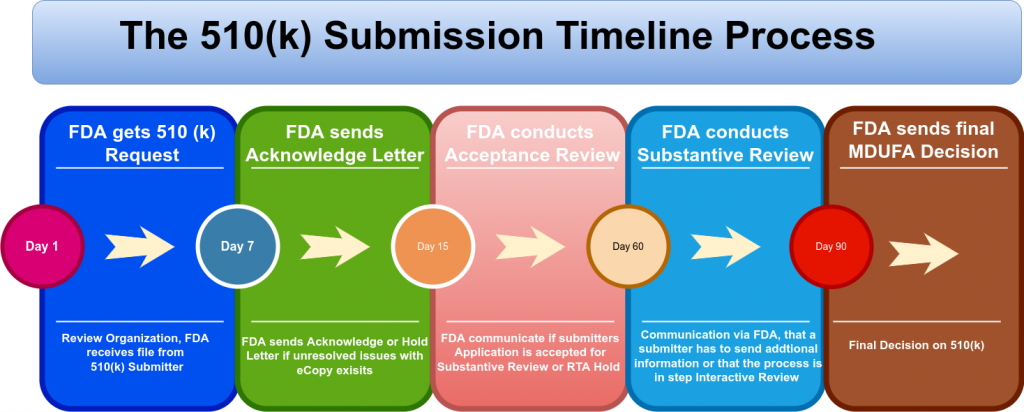
Folgende IT-Services zum Thema Medical Device 510 (K) Approval erhalten Sie von uns:
- Beratung und Unterstützung bei der Vorbereitung und Einreichung von 510(k) Benachrichtigungen
- Überprüfung von technischen Dokumentationen, um sicherzustellen, dass sie den Anforderungen der FDA entsprechen
- Erstellung von Testplänen und -protokollen für medizinische Geräte
- Durchführung von Tests und Bewertungen, um die Sicherheit und Wirksamkeit von Geräten zu beurteilen
- Unterstützung bei der Beantwortung von Fragen oder Anforderungen der FDA während des Bewertungsprozesses
- Bereitstellung von Schulungen und Workshops für Hersteller und Mitarbeiter, um sie über die Anforderungen und Best Practices im Zusammenhang mit dem 510(K) Prozess zu informieren.
- Die Schulung “510(k) FDA-Zulassung und Cybersecurity”, können Sie auf der Seite www.Blueguardtraining.com buchen.
